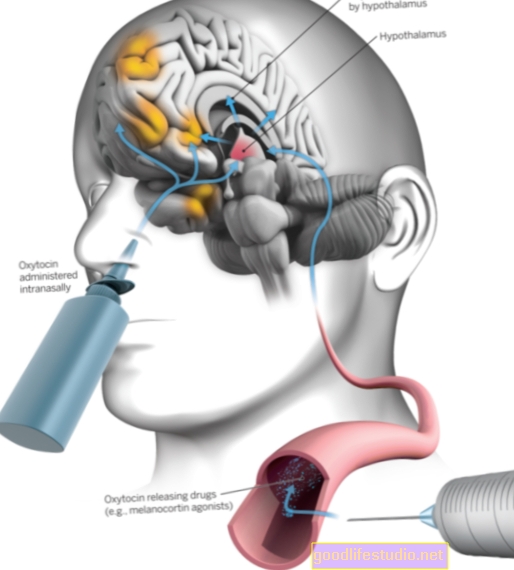
„Spravato“: naują ketamino gydymą turi patvirtinti FDA
Praėjusią savaitę JAV maisto ir vaistų administracijos (FDA) komitetas per 14-2 balsų rekomendavo agentūrai patvirtinti esketamino (tam tikros rūšies ketamino) nosies purškalo vartojimą gydymui atsparios depresijos ir tam tikros kitos depresijos rūšys.
Gydymui atspari depresija yra tada, kai klinikinė depresija nereaguoja į kelis (bent du) bandymus ją gydyti bent dviejų skirtingų rūšių vaistais ar psichoterapija per metus ar ilgiau.
Jei FDA baigs patvirtinti vaistą - ir mes tikime, kad taip bus - nosies purškalas suteiks naujos vilties depresija sergantiems žmonėms.
Ketaminas neseniai buvo skiriamas be recepto depresijai gydyti brangių „ketamino klinikų“. Tokios klinikos žmonėms reguliariai ima 650–1200 USD už gydymą, daugumai žmonių norint pradėti reikia 6–8 gydymo būdų. Dauguma draudimo nepadengs šio gydymo išlaidų, nes depresija nėra sąlyga, kad ketaminas šiuo metu yra patvirtintas gydyti.
Geroji žinia
Naujasis vaistas pavadintas „Spravato“, esketamino intranazaline forma, jį gamina „Janssen“, „Johnson & Johnson“ padalinys. Galutinis FDA patvirtinimas dėl tokio tipo ketamino vartojimo padarytų tokį gydymą kur kas labiau prieinamą daugiau žmonių.
Komitetas nustatė, kad „Spravato“ yra palankus naudos ir rizikos santykis, išanalizavęs penkių skirtingų tyrimų, atliktų pacientams, sergantiems gydymui atsparia depresija, saugumo ir veiksmingumo duomenis. Tyrimas parodė, kad esketaminas, tiekiamas per nosies purškalą kartu su tradiciniu geriamuoju antidepresantu, statistiškai reikšmingai pagerino su depresija susijusius simptomus.
Istoriškai FDA retai prieštarauja savo psichofarmakologinių vaistų patariamajam komitetui. FDA šaltinis man pasiūlė, kad FDA patvirtintų vaistą šioms specifinėms sąlygoms.
FDA greitai patvirtino šį vaistą, nes jis jau yra patvirtintas naudoti kitiems medicinos poreikiams kaip anestetikas. Todėl jo saugos profilis taip pat gerai suprantamas. FDA šį greitą procesą vadina „proveržio terapijos“ pavadinimu.
FDA komitetas taip pat patvirtino „Spravato“ dėl didelės depresijos sutrikimo žmonėms, kuriems gresia tiesioginė savižudybės grėsmė.
Bloga žinia
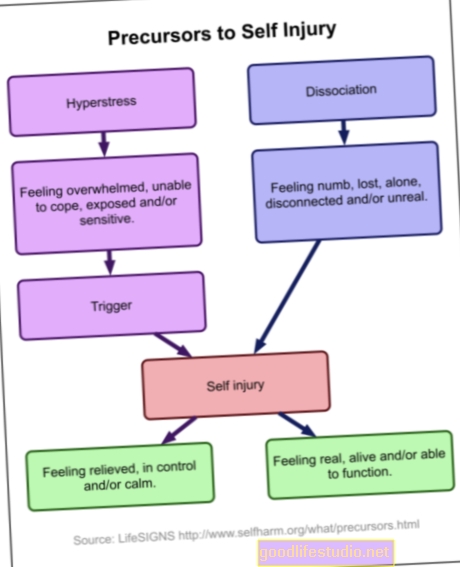
Paprastai paternalistiškai, FDA komitetas nemanė, kad pacientams gali būti patikėta vartoti vaistą, kaip nurodyta patiems. Vienas iš šalutinių poveikių po Spravato vartojimo yra atsiribojimas ir sedacija. Akivaizdu, kad nenorėtumėte, kad kas nors išgertų šio vaisto dozę ir eitų valdyti sunkiųjų mašinų.
Taigi komitetas rekomenduoja FDA neleisti pacientams vartoti nosies purškalo namuose, teigia „Vantage“:
Agentūra pasiūlė rizikos vertinimo ir sušvelninimo strategiją, pagal kurią reikalingas savarankiškas gydymas sveikatos priežiūros įstaigoje, kuri dvi valandas gali stebėti pacientus, kol nepraeis disociacinis ir sedacinis šalutinis poveikis, taip pat pacientų registrą, kuris galėtų padėti apibūdinti projekto riziką. .
Tai reiškia, kad kiekvienam gydymui pacientai vis tiek turės susitarti su savo vaistų tiekėju ir dvi valandas (??!) Pabūti kabinete (?) Po to, kai jie išgers vaistą. Tai yra keista rekomendacija ir gali sutramdyti žmonių norą išbandyti vaistą. Tikiuosi, kad galutinis FDA patvirtinimas padarys programą lankstesnę ir atsižvelgs į įvairius žmones, kenčiančius nuo depresijos, nes šie reikalavimai labiausiai paveiks mažas pajamas gaunančius žmones.
Bet tai atitinka ketamino klinikų veiklą šiuo metu. Ten ketaminas infuzuojamas į veną (IV) tiesiai į kraują. Pacientas gauna infuziją, tada jis turi laikytis maždaug valandą, kad būtų galima stebėti, ar nėra neigiamo šalutinio poveikio.
Infuzijos taip pat leidžia vaistui apeiti kepenų ir kitų organų apdorojimą. Intranazaliniai purškalai leidžia tą patį apeiti, todėl lengviau pasiūlyti vaistą mažesnėmis dozėmis, išlaikant jo veiksmingumą. Be to, kadangi nereikia IV, tikimasi, kad „Spravato“ bus siūloma už prieinamesnę kainą, nei daro dabartiniai ketamino vaistai nuo depresijos.
Tikiuosi, kad „Janssen“ šį vaistą kainuoja pakankamai brangiai, kad dauguma paprastų amerikiečių galėtų juo naudotis. Šiandien dauguma amerikiečių negali sau leisti įvažiuoti į ketamino klinikas. Taip pat raginu sveikatos draudimo bendroves nedelsiant patvirtinti šio vaisto aprėptį visuose jų siūlomuose sveikatos planuose, atsižvelgiant į konkrečias patvirtintas sąlygas, nes tai gali pakeisti žaidimą, padedant žmonėms jaustis geriau nuo sunkių depresijos simptomų.
FDA ketina priimti sprendimą iki 2019 m. Kovo 4 d. Tikimės, kad agentūra teisingai pasielgs milijoną + amerikiečius, kenčiančius nuo atsparios gydymui ir kitų sunkių depresijų rūšių. Mes taip pat tikimės, kad agentūra sumažins gydymo kliūtis, pavyzdžiui, reikalaudama apsilankyti pas gydytoją, kad gautų šį svarbų depresijos gydymą.
Daugiau informacijos
Iš „Vantage“: Esketaminas plūduriuoja praėjus „Adcom“ balsavimui
Iš „Pharma Letter“: „J&J“ nosies purškalas laimėjo pirmąjį pritarimą ketaminu pagrįstų depresijos tyrimų metu