Leidinys vėlgi šališkas, šį kartą skirtas antipsichotikams

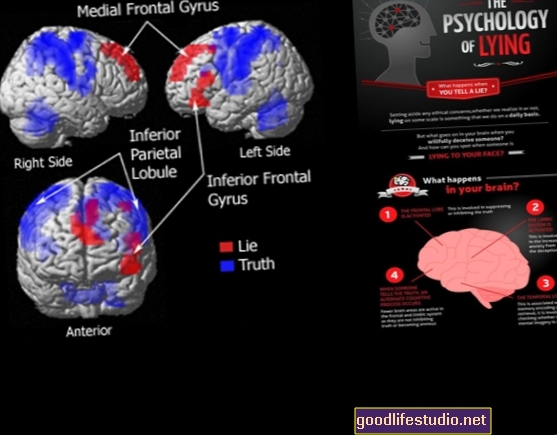
Antidepresantai ypač nukentėjo žiūrint į FDA išankstinio patvirtinimo tyrimus. Tiesą sakant, naujausiame Lesley Stahl 60 minučių ataskaita apie antidepresantų tyrimus, ji nuėjo visiškai suglumusi viso to prasmės. Ką tai reiškia, kai tyrėjai randa tokių neigiamų išvadų, kurios niekada nebuvo paskelbtos?
Išsiaiškinkime…
Dabartinio tyrimo metu mokslininkai ištyrė 24 FDA išankstinės rinkodaros tyrimus aštuoniems antrosios kartos antipsichotikams (dar vadinamiems netipiniais antipsichotikais):
- aripiprazolas („Abilify“)
- iloperidonas („Fanapt“)
- olanzapinas (Zyprexa)
- paliperidonas („Invega“)
- kvetiapinas (Seroquel)
- risperidonas (Risperdal)
- risperidono ilgai veikianti injekcija (Consta)
- ziprasidonas („Geodon“)
Tuomet mokslininkai palygino FDA apžvalgos dokumentų rezultatus su medicinos žurnaluose pateiktais rezultatais. Idealiu atveju jie tikėtųsi rasti 24 paskelbtus tyrimus, tačiau vietoj jų galėtų rasti tik 20:
[... F] mūsų FDA pateikti išankstinės rinkodaros tyrimai, kurie davė nemalonių rezultatų, liko nepaskelbti. Trys parodė, kad naujieji antipsichoziniai vaistai neturėjo reikšmingo pranašumo prieš placebą.
Ketvirtajame vaistas buvo pranašesnis už placebą, tačiau jis gerokai nusileido daug pigesniam konkuruojančiam vaistui, pažymi mokslininkai.
Tik 17 procentų tyrimų nebuvo paskelbta, o tai iš tikrųjų yra mažesnė nei pramonės vidurkis naujiems vaistų patvirtinimams, kylantiems per FDA procesą.
Ir tai nėra taip blogai, kaip duomenys - 40 procentų tyrimų niekada nebuvo paskelbta - apie antidepresantus:
1998 m. Moore pasinaudojo Informacijos laisvės įstatymu, kad išviliotų tokius duomenis iš FDA. Iš viso buvo atlikti 47 kompanijos remiami tyrimai - apie „Prozac“, „Paxil“, „Zoloft“, „Effexor“, „Serzone“ ir „Celexa“. (Be to, paaiškėjo, kad apie 40 proc. Klinikinių tyrimų niekada nebuvo paskelbta. Tai yra žymiai daugiau nei kitų klasių vaistams, sako Lisa Bero iš Kalifornijos universiteto San Franciske; apskritai 22 proc. Klinikinių tyrimų narkotikų bandymai neskelbiami. „Apskritai, - sako Kirschas, - neskelbti tyrimai buvo tie, kurie neparodė reikšmingos naudos vartojant tikrąjį vaistą.“)
Kiek daugiau nei pusėje paskelbtų ir nepaskelbtų tyrimų jis ir jo kolegos pranešė 2002 m., Vaistas depresiją palengvino ne geriau nei placebas. "O papildoma antidepresantų nauda buvo dar mažesnė, nei matėme analizuodami tik paskelbtus tyrimus", - prisimena Kirschas. Maždaug 82 procentus atsako į antidepresantus, o ne 75 procentus, kuriuos jis apskaičiavo, nagrinėdamas tik paskelbtus tyrimus, taip pat pasiekė manekeno tabletės.
Svarbus dalykas, kurį reikia nepamiršti, yra tai, kad išankstiniai rinkodaros tyrimai pirmiausia atliekami siekiant gauti vaistą per FDA procesą. Tai nėra galutinis žodis apie vaisto veiksmingumą, tai tiesiog biurokratinė kliūtis, kurią kompanijos turi kirsti, kad galėtų patekti į savo rinką.
Patekę į rinką, atliekama dešimtys papildomų tyrimų, o antidepresantų atveju - šimtai. Šie tyrimai, kurie dažnai būna įvairesni, nepriklausomi ir atliekami įvairesnių tyrėjų, galiausiai sudaro didžiąją dalį vaisto veiksmingumo tyrimų.
Taigi šio naujausio tyrimo sidabro pamušalas yra tas, kad niekada nepaskelbtų tyrimų procentas yra iš tikrųjų žemesnis nei pramonės vidurkis ir žymiai mažesnis nei tyrimų, kurie niekada nebuvo paskelbti prieš patvirtinant antidepresantus, skaičius.
Nuoroda
Turneris, E. H., Knoepflmacher, D. ir Shapley, L. (2012). Publikacijos šališkumas antipsichoziniuose tyrimuose: efektyvumo analizė, palyginant paskelbtą literatūrą su JAV maisto ir vaistų administracijos duomenų baze. PLoS medicina, 9 (3): e1001189. doi: 10.1371 / journal.pmed.1001189